Em agosto de 2025, o Senado aprovou três nomes para a diretoria colegiada da Agência Nacional de Vigilância Sanitária (Anvisa), incluindo o novo diretor-presidente, o economista Leandro Safatle, que passou a ocupar o cargo após o fim do mandato de Antônio Barra Torres.
Safatle assumiu a presidência da Anvisa em um momento de grandes transformações no setor regulatório sanitário, onde o ritmo de descobertas, sobretudo em saúde, é intenso, mas os processos de análise e aprovação dentro da própria agência seguem a passos mais lentos.
Em entrevista exclusiva à Agência Brasil, o novo diretor-presidente conversou sobre as principais inovações nacionais em saúde, sobretudo do ponto de vista do Sistema Único de Saúde (SUS). “Ainda temos muita inovação vinda de fora. Agora, estamos lidando com inovação feita no país”, disse.
Safatle comentou ainda sobre o recém-criado Comitê de Inovação, com foco em temas considerados prioritários para a Anvisa; sobre um processo interno para otimizar filas de análises processuais; e sobre a possibilidade de a agência se consolidar como autoridade sanitária de referência nas Américas e globalmente.
Confira os principais trechos da conversa:
Agência Brasil: A Anvisa autorizou este mês o início da primeira fase de estudos clínicos com a polilaminina , medicamento desenvolvido por pesquisadores brasileiros para tratar lesão na medula. O que a gente pode esperar desses estudos e quais os próximos passos?
Leandro Safatle: Estamos falando de uma pesquisa nacional feita por uma pesquisadora de uma universidade pública. Com inovação nacional, cientista nacional, desenvolvimento nacional, todo um processo de desenvolvimento feito no país, e isso é muito importante. No setor saúde, a gente ainda tem muita inovação vinda de fora. Agora, estamos lidando com inovação feita no país. A indústria está fazendo inovação no país. Hoje, isso é um fato bastante importante para atender demandas do país. Esse é um desses casos.
Um laboratório nacional encampou esse projeto. Protocolaram o pedido de início de estudo de pesquisa clínica na Anvisa. Foi aprovada a fase 1, que tem o objetivo de focar na segurança do produto. São cinco pacientes que vão fazer parte desse estudo. Aprovando a fase 1, vem a fase 2, a 3, onde vamos avaliar questões como a eficácia do produto de fato, além de aprofundar mais na segurança. Precisa passar por esse ciclo regulatório completo para conseguir o registro na Anvisa. É um assunto promissor. Há fortes indícios de que o produto pode ter um segmento importante no decurso de pessoas que têm lesão medular.
É difícil falar de prazo porque estamos falando de inovação, de estudo clínico. E o estudo clínico leva seu tempo. O que eu posso dizer é que a Anvisa vai dar a celeridade necessária para o avanço desse projeto. Será prioridade.
Agência Brasil: A Anvisa realizou, em dezembro, a primeira reunião do Comitê de Inovação, criado para acompanhar e avaliar produtos e tecnologias inovadores considerados prioritários para a saúde pública brasileira. Como esse comitê vai atuar e quais os temas considerados prioritários?
Safatle: O comitê está pegando casos de inovação que estão acontecendo no país, projetos importantes que têm impacto, principalmente, na saúde pública. Selecionamos quatro produtos que estão dentro desse comitê: a polilaminina, a vacina contra o Chikungunya, o método Wolbachia para combate à dengue e endopróteses. A gente está acompanhando esses quatro casos.
Já tivemos reunião para tratar desses temas e a ideia é que a gente acompanhe e dê o apoio necessário para que a equipe técnica faça a melhor análise possível. É um comitê que puxa, para a alta gestão da Anvisa, o trabalho de acompanhar os casos. E que vai dar o apoio necessário, o subsídio necessário para que a área técnica faça o melhor trabalho possível de avaliação.
Agência Brasil: Por que a escolha dessas quatro inovações?
Safatle: A gente tem alguns estudos, em fase inicial, de inovação radical nacional. São casos que tratam desses temas. É inovação feita no país, com desenvolvimento feito no país. Por isso, foram selecionados. Trata-se de inovação importante, que pode ter uma repercussão grande em termos de saúde pública.
Agência Brasil: Em dezembro, a Anvisa aprovou uma proposta com medidas excepcionais e temporárias para otimizar a fila de análises processuais. A expectativa é reduzir as filas pela metade em seis meses e normalizar os pedidos em um ano. Como vai funcionar esse processo?
Safatle: Nós colocamos essa questão da fila de análises processuais da Anvisa como uma das prioridades para que a gente possa atuar ao longo desse ano. Foi feita a aprovação, por meio de uma RDC [resolução da Diretoria Colegiada], de uma série de medidas para a gente poder acelerar essas filas, principalmente filas de medicamentos, vacinas, dispositivos médicos, filas de inspeção. O que a gente quer? A gente quer trazer melhores prazos. A gente viu que havia um processo, de certa forma, demorado para poder aprovar essas novas tecnologias. Elaboramos uma série de medidas para poder reduzir esses prazos.
Essas medidas envolvem força-tarefa dentro da casa, para poder agilizar esses processos; aproveitar parte de estudos clínicos feitos fora, que a gente chama de reliance (confiança regulatória), aproveitando parte da documentação que é feita fora; análises otimizadas que agregam vários produtos, fazendo análises conjuntas no intuito de ganhar tempo. Estamos com uma série de instrumentos para cada uma das filas, para ver de que forma a gente consegue atuar para poder mitigar esse problema.
Ao mesmo tempo, temos uma sala de situação dentro da agência que acompanha diariamente a evolução das filas. Já temos alguns resultados importantes de redução de fila e de tempo de análise. A ideia é fazer uma gestão regulatória ágil, para poder dar respostas mais rápidas para essas questões. Também criamos um comitê de monitoramento dessas medidas para que esse processo todo seja acompanhado pela sociedade civil e pelo setor regulado, para dar a devida transparência para essas ações.
Agência Brasil: Para que fique claro: a proposta não é afrouxar as regras em relação às análises processuais, mas dar celeridade, fazer andar mais rápido?
Safatle: Isso. São medidas temporárias. Temos o prazo de um ano para executá-las. Mas o processo de análise permanece o mesmo. As regras não estão sendo afrouxadas ou nada nesse sentido. O rigor científico e a segurança sanitária são primazia na agência, são o que traz confiança da sociedade para o trabalho da agência. Nesse sentido, a gente segue stricto sensu a questão da segurança sanitária. O que estamos fazendo é mecanismo de gestão. Gestão de pessoas, gestão de processos, para otimizar o tempo, a análise e fazer força-tarefa.
Tivemos um concurso importante. No fim do ano passado, foram chamados 100 especialistas da Anvisa. O curso de formação terminou, e essa turma deve ser nomeada agora, entre janeiro e fevereiro. É o maior reforço que a Anvisa já teve nos últimos dez anos. A ideia é que esses 100 entrem já para ajudar nesse processo de redução das filas, prioritariamente. Que eles entrem nesse esforço que a casa inteira está fazendo para redução das filas.
Agência Brasil: Sobre essa questão do rigor técnico, a Anvisa tem como meta, para 2026, o reconhecimento internacional, a consolidação da agência como uma autoridade sanitária de referência?
Safatle: Esse é um ponto muito importante. A Anvisa está sofrendo um processo de qualificação neste momento por parte da Organização Mundial da Saúde (OMS). Nós já somos uma agência de referência, mas, agora, estamos passando por um processo de qualificação como as principais agências do mundo passaram, estão passando ou vão passar em breve.
Estamos num empenho muito grande para poder seguir bem nesse processo de qualificação. A ideia é que, com essa qualificação, a OMS reconheça a Anvisa como uma agência de referência. Isso é muito importante para o Brasil, no sentido de ter uma agência de referência, para a região das Américas e para o mundo.
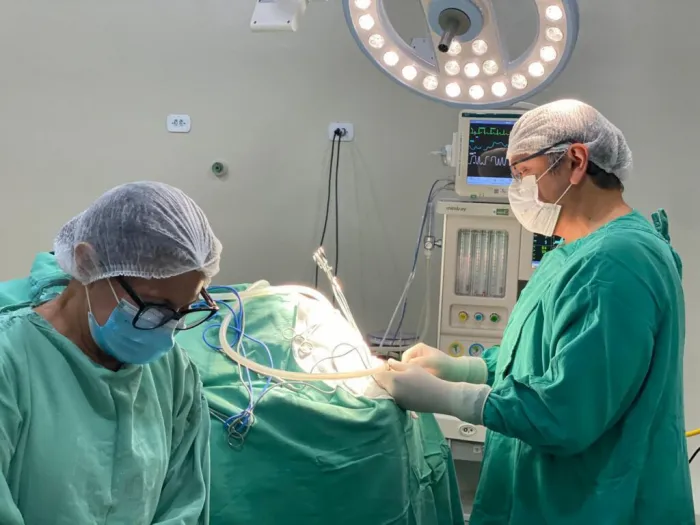 Piauí Serviço de neurocirurgia completa quatro anos com mais de 12 mil atendimentos de urgência no Hospital Regional de Parnaíba
Piauí Serviço de neurocirurgia completa quatro anos com mais de 12 mil atendimentos de urgência no Hospital Regional de Parnaíba  Saúde Quiet luxury redefine estética com foco na naturalidade
Saúde Quiet luxury redefine estética com foco na naturalidade  Piauí Governo do Piauí implanta comitê para prevenção do suicídio
Piauí Governo do Piauí implanta comitê para prevenção do suicídio Mín. 22° Máx. 29°